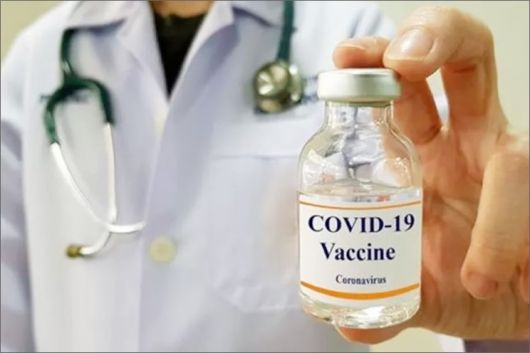
As pesquisas de vacinas para combater o novo coronavírus terão pelo menos 28 mil voluntários no Brasil, é o que mostram os dados divulgados pelas empresas responsáveis pelos quatro testes já aprovados pela Agência Nacional de Vigilância Sanitária (Anvisa). Ao menos outras duas também já estão na fila e poderão ser testadas em breve.
A Pfizer, responsável por uma das pesquisas, teve autorização para dobrar o número de voluntários para 2 mil. A fase três de estudos clínicos da empresa acontece em São Paulo e na Bahia.
A pesquisa com mais candidatos até agora no país é a da vacina desenvolvida pela Universidade de Oxford, em parceria com a farmacêutica AstraZeneca. O grupo teve recentemente aprovado, com aval da Anvisa, o aumento de 5 mil para 10 mil participantes, depois de um pedido da Universidade Federal de São Paulo (Unifesp), responsável pela coordenação desses estudos no país. Ao menos 4,6 mil já receberam a vacina.
A CoronaVac, fruto de uma parceria entre o instituto Butantan e a farmacêutica chinesa Sinovac, tem 9 mil voluntários e, segundo o instituto, ao menos 4 mil já receberam uma ou duas doses da vacina. O instituto deve iniciar, em novembro, obras em sua fábrica para ampliar a capacidade de produção das vacinas, com previsão de finalização a partir de setembro do ano que vem. A expectativa é de produzir mais de 100 milhões de doses da CoronaVac por ano a partir de 2022.
Em agosto a Anvisa autorizou os testes da fase 3 da vacina da Johnson & Johnson no Brasil, com 7 mil voluntários em São Paulo, Rio Grande do Sul, Minas Gerais, Rio de Janeiro, Paraná, Rio Grande do Norte e Bahia.
Há expectativa de que esse número aumente com a aprovação dos testes de ao menos outras duas vacinas: uma delas é da Dasa, grupo que reúne 40 redes de laboratórios de medicina diagnóstica, e será desenvolvida pela empresa Covaxx. Os testes foram iniciados no mês passado, em Taiwan.
Já a vacina russa Sputnik V também deve ter testes em breve. O governo do Paraná anunciou que submeteu à Anvisa o protocolo de validação da fase de estudos clínicos da vacina e a previsão é de início dos testes até o final de outubro.
 ESPORTE / PORTO
ESPORTE / PORTO SEGURANÇA EM EUNÁPOLIS
SEGURANÇA EM EUNÁPOLIS ANIVERSÁRIO / PORTO SEGURO
ANIVERSÁRIO / PORTO SEGURO